类器官的建立及其应用研究进展
类器官(Organoid)是指在体外用3D培养技术对干/祖细胞进行诱导分化形成的在结构和功能上都类似于靶器官/组织的三维细胞复合体。类器官其具有稳定的表型和遗传学特征,能够在体外长期培养。
2009年,荷兰科学家Hans Clevers首次在体外通过三维培养成体干细胞培育出拥有隐窝和绒毛结构的小肠细胞模型。这种体外三维(3D)培养成体干细胞或多能干细胞的技术被称之为“类器官”(Organoids)技术,因为所培养的组织类似物具有一定空间结构,并能模拟真实器官部分功能。
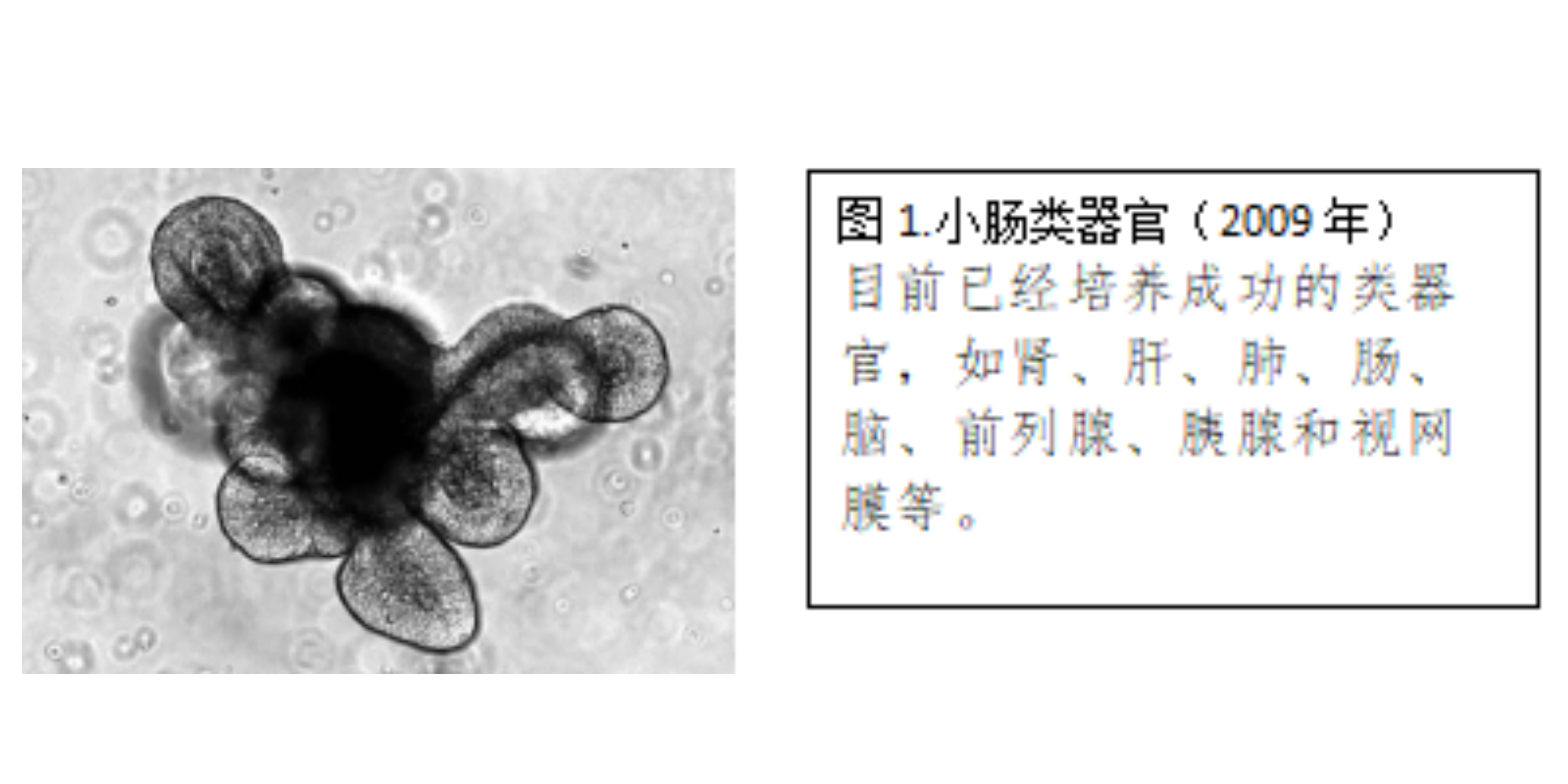
一、类器官的种类
1、组织细胞来源类器官:如肿瘤组织培养产生的类器官。
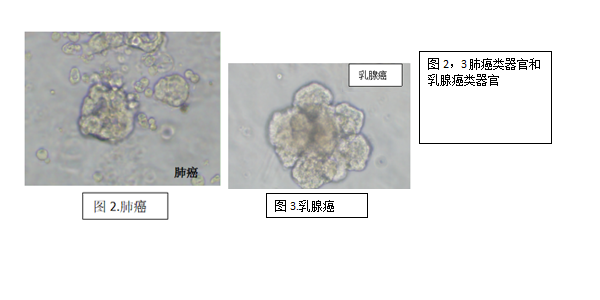





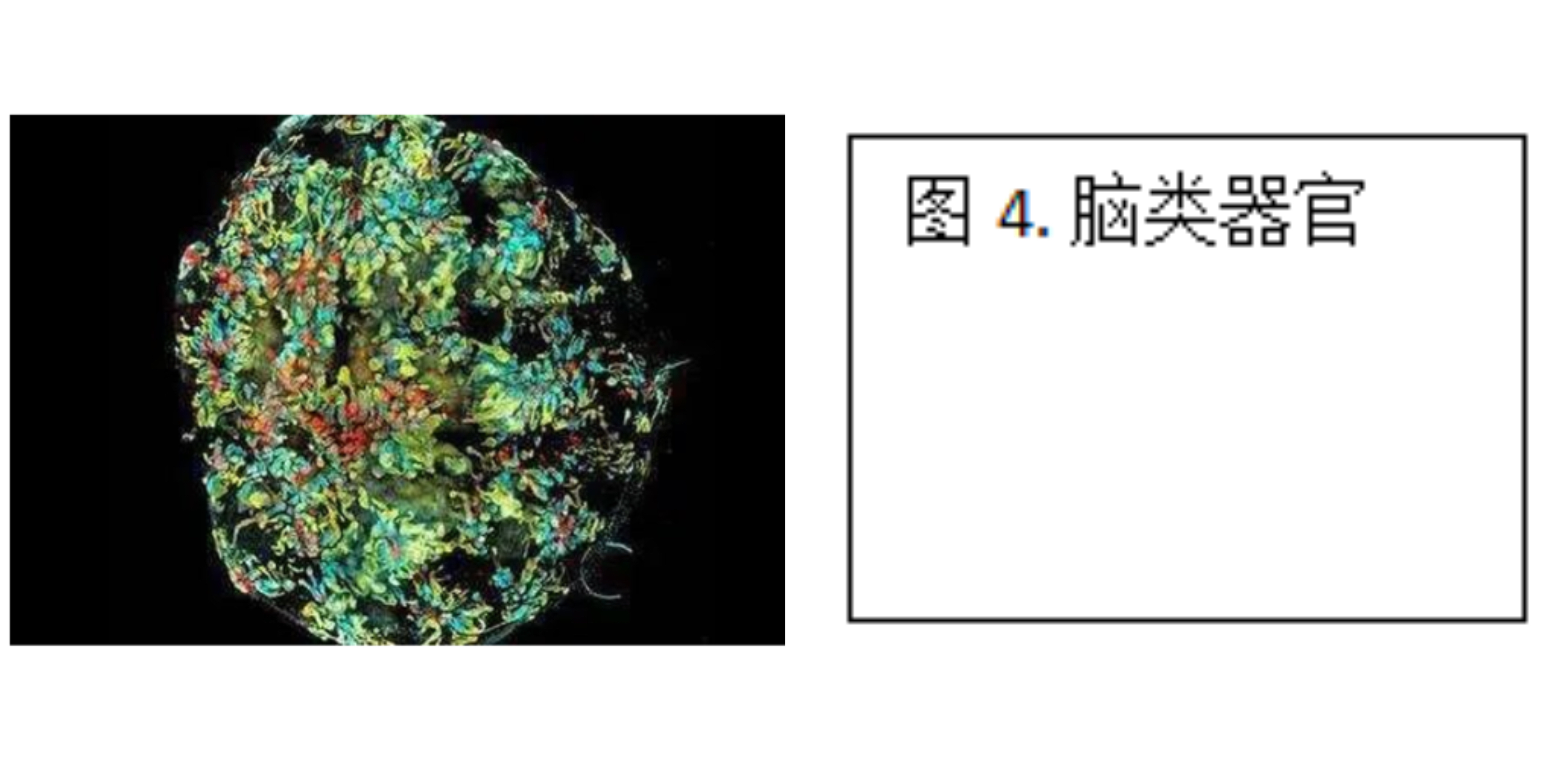
 2、多能干细胞来源类器官:如大脑(brain)、视杯(Optic Cup)、内耳(Inner Ear)、肺(lung)、肝(liver)、结肠(Colon)、肾(Kidney)、胰腺(Pancreatic)、前列腺(Prostate)、胃(Gastroids)、乳(galactophore)等
2、多能干细胞来源类器官:如大脑(brain)、视杯(Optic Cup)、内耳(Inner Ear)、肺(lung)、肝(liver)、结肠(Colon)、肾(Kidney)、胰腺(Pancreatic)、前列腺(Prostate)、胃(Gastroids)、乳(galactophore)等


二、类器官的构建和评估
1、类器官的构建:是一项系统工程,需要物质基础和特定的培养环境。类器官构建的物质基础。
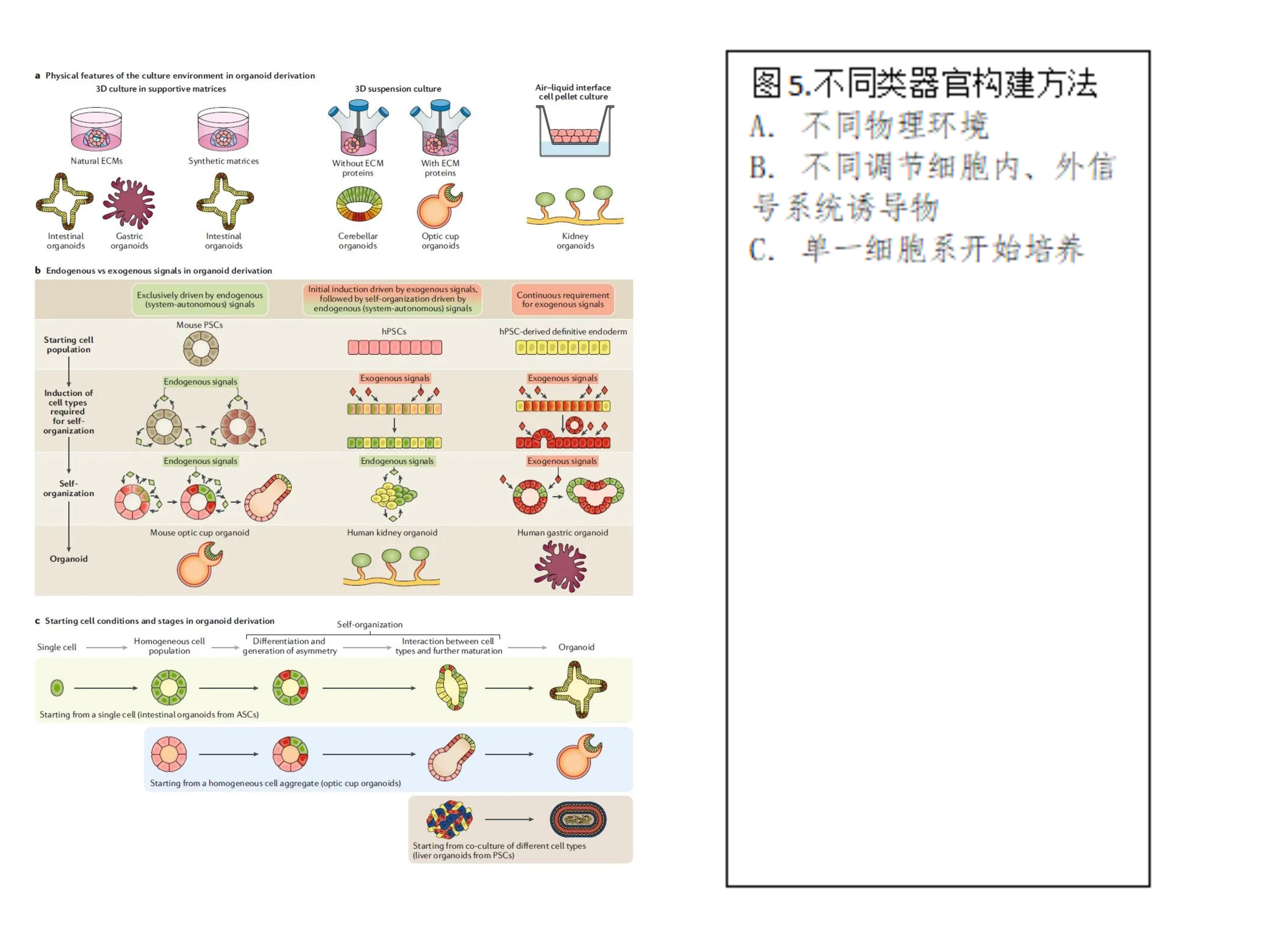
1.1 3D支架:3D支架给细胞的生长与细胞类别的自我组织及空间结构构建提供支撑,在细胞团的作用下,因为不同细胞会分泌不同的细胞粘附因子,不同类型的细胞会运动到3D支架的不同位置,实现了细胞类型的分离。不同的特定物理环境,可以包括采用天然细胞外基质(ECM,如类小肠器官或类胃器官)或合成高分子(如类小肠器官)的3D支架进行静态培养、采用无细胞外基质支架支撑(如类脑器官)或含细胞外基质蛋白(如类视网膜器官)的3D悬浮搅拌式培养、或者是采用气-液界面细胞团培养(如类肾器官)。
1.2 特殊培养基:培养基含有各种生长因子的培养基及和诱导添加物如FGF、EGF以及干细胞、支持细胞或组织等;而特定的培养环境包括了调控氧气(如低氧)、温度、二氧化碳、甚至包括一些力学等模拟体内细胞生长环境的参数。不同诱导物添加策略,包括全内源性诱导自主装(如类视网膜器官)、外源诱导分化-内源自组织(如类肾器官)或全外源诱导自主装(如类胃器官)。
1.3 特殊的培养微环境:类器官的培养过程是一个精准调控细胞生长微环境的过程,根据提供个性化的培养条件来模拟细胞在体内的微环境。由于空间的限制形成了“谱系定向”,也就是“空间限制引起的细胞命运决定”。而相应的培养基及诱导物激活或者抑制参与类器官形成的特定信号通路与稳态的维持。因此,在空间约束作用以及原来细胞分泌物或添加的诱导物的刺激等,这些细胞被进一步的分化,最终形成类器官。
起始细胞状态,可以选择单细胞(如类小肠器官)、均质的细胞团(如类视网膜器官)或多细胞类型的细胞团(如类肝细胞)。

 2、类器官的评估:
2、类器官的评估:
类器官需要与常规培养的细胞对比,需要保持生物一致性,包括细胞形态、免疫组化、功能、表观遗传学及基因表达的一致性。如肿瘤类器官要确定类器官和原肿瘤的一致性,运用组织病理学染色和基因测序的方法对培养的类器官与原代肿瘤标本进行对比,显示构建的类器官依然保留着原肿瘤的特性。

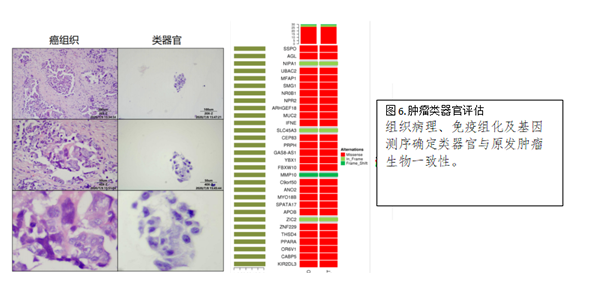


三、类器官的应用
类器官技术在疾病建模、药物筛选、精准医疗、器官发育、再生医学等领域都有广泛的应用前景。
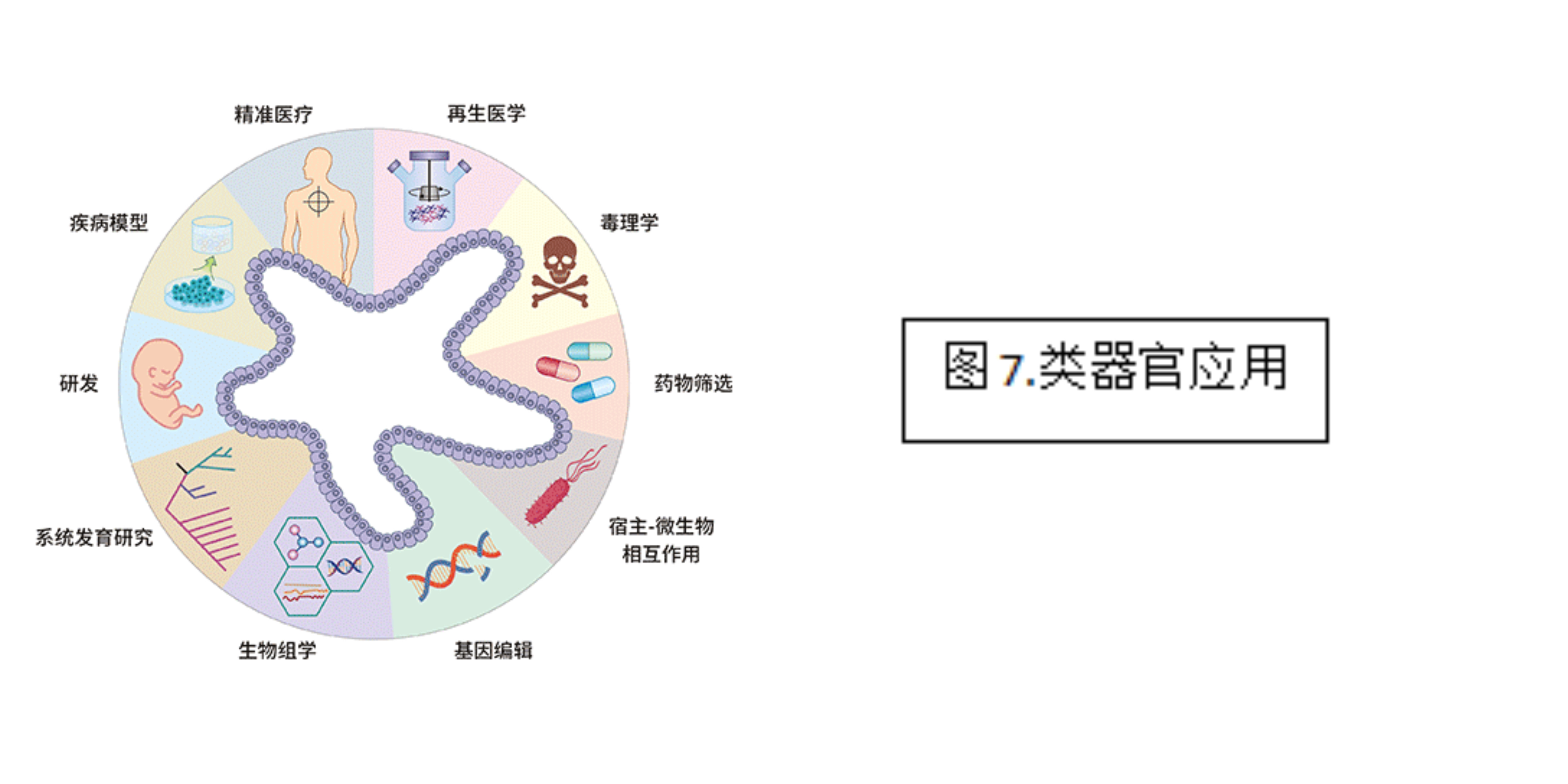


例如肿瘤筛选、药物敏感检测等类器官目前可筛选的药物种类包括化疗药、小分子靶向药、抗体药物等。通过检测药物的IC50和细胞抑制率,来预测对肿瘤抑制效果最好的药物或药物组合。
肿瘤临床药筛模型必须能满足三大要求包括:需要在短时间内出具药敏检测结果、药物筛查通量高、预测效果准确。而类器官都显现出了强劲优势。
速度快:类器官构建成功率高,培养速度快。常规来说,在类器官培养一周之后就可以进行药筛。从样本采集到出具药敏结果的全流程已经可以很好地控制在2周之内。
通量高:利用类器官不仅可以在孔板上进行多种药物的筛查,每个药物还可以测试不同的浓度,多个实验平行开展。
临床相关性强:类器官用于癌症药筛的临床相关性和预测有效性在多篇研究中都已经得到了较为充分的证实。Vlachogiannis G团队在Science发表了肿瘤类器官体外药敏测试指导临床用药的里程碑式研究,在71位转移性胃肠道癌提取了110份组织构建了类器官,共测试了55种抗癌药物。研究结果显示,类器官药筛达到了93%的特异性,100%的灵敏度、88%的阳性预测率和100%的阴性预测率,展现了极高的临床相关性。
利用肿瘤类器官还可以构建多种肿瘤的生物信息库平台,并利用类器官模型库进行大规模药物候选分子的敏感性检测,建立药效学和临床用药信息数据库,这将加速癌症患者精准化、个体化治疗的进程。
四、类器官临床应用面临的挑战
目前,大多数类器官本身不具备血管化结构和免疫环境,因此无法预测抗血管生成类和免疫类药物。且目前的类器官仅能检测出药物对于肿瘤的抑制效果,对于其他器官是否存在副作用和安全性风险并不能做出预判。
4.1 类器官临床应用的困境:
血管化:目前大多类器官本身并不具备血管化的结构。因此,随着类器官体积的增长,类器官受限于氧气的缺失以及代谢废物的增加,可能导致的组织坏死。已有研究构建血管内皮细胞微环境的肿瘤类器官,将类器官肿瘤细胞和血管内皮细胞在Matrigel上共同培养,生成血管结构以期解决类器官血管化缺失的问题。
免疫化:血管化以外的难点还包括模拟肿瘤和免疫环境的相互作用关系。2019年Nature Protocol发表了肿瘤类器官和免疫细胞共同培养的相关protocol,可以体现和模拟出肿瘤微环境的部分特征。以上皮类器官和免疫细胞共培养模型为例,可通过在培养基中添加活化的免疫细胞、在组织消化成单细胞后和免疫细胞共同生长、添加ECM中的重组细胞因子等方法重塑类器官和免疫细胞的相互作用。
系统化:相比于单个类器官,类器官系统的构建能够对药物疗效和潜在毒性做出更完整全面的评估。目前类器官仅能检测出药物对于肿瘤的抑制效果,对于其他器官组织是否存在其他副作用和安全性风险并不能做出预判。
4.2 国家高度重视:2021年初,“基于类器官的恶性肿瘤疾病模型”在科技部下发的《关于对“十四五”国家重点研发计划6个重点专项2021年度项目申报指南征求意见的通知》中被列为首批启动的“十四五”国家重点研发专项任务。“十四五”国家重点研发计划指出,类器官是一项重大的技术突破,用于疾病模型的建立,还可用于研究病理状态下干细胞变异、异质性及其发生机理,挖掘疾病诊疗的新靶标和探索诊疗新策略。从类器官技术逐渐被各大顶级期刊报道到科技部下发的文件,我们可以看到类器官技术在未来将有非常大的应用价值和发展前景。
参考文献
1.Puschhof J,et al.Intestinal organoid cocultures with microbes. Nat Protoc. 2021 Oct;16(10):4633-4649
2.Drost J, Clevers H.Organoids in cancer research. Nat Rev Cancer. 2018 Jul;18(7):407-418.
3.Revah O,et al.Maturation and circuit integration of transplanted human cortical organoids .Nature . 2022 Oct;610(7931):319-326.
4.Lewis SM,et al.Clinical applications of 3D normal and breast cancer organoids:A review of concepts and methods.Experimental Biology and Medicine 2022; 247: 2176–2183
5.LeSavage BL,et al.Next-generation cancer organoids. Nat Mater. 2022 Feb;21(2):143-159.
6.Dekkers JF,et al.Uncovering the mode of action of engineered T cells in patient cancer organoids. Nat Biotechnol. 2023 Jan;41(1):60-69.
7.Jalan-Sakrikar N,et al.Organoids and regenerative hepatology. Hepatology. 2023 Jan 1;77(1):305-322.
8.Corsini NS, Knoblich JA.Human organoids: New strategies and methods for analyzing human development and disease.Cell. 2022 Jul 21;185(15):2756-2769.
9.Yang R, Yu Y.Patient-derived organoids in translational oncology and drug screening. Cancer Lett. 2023 May 28;562:216180.
10.Hillion K,et al.Redesigning hydrogel geometry for enhanced organoids. Nat Methods. 2022 Nov;19(11):1347-1348
作者:程保合 山东省干细胞学会干细胞知识科普特聘专家(济南至晟生物科技有限公司)

